Nanotechnologies & santé
Invisibles à l’œil nu, mesurant entre 1 et 100 nanomètres, les nanoparticules révolutionnent actuellement la médecine. Pour visualiser cette échelle, imaginez qu’un nanomètre est à un mètre ce qu’une bille est à la Terre : un rapport de un à un milliard. À cette dimension, les matériaux acquièrent des propriétés physiques, chimiques et optiques radicalement différentes de leur forme macroscopique, ouvrant des possibilités thérapeutiques et diagnostiques inédites.
Les nanotechnologies médicales se déploient aujourd’hui sur quatre fronts majeurs. Elles permettent de détecter les maladies bien avant l’apparition des symptômes, d’observer les processus biologiques à l’échelle moléculaire avec une précision inégalée, d’acheminer les médicaments exactement là où le corps en a besoin, et même de combiner diagnostic et traitement en une seule intervention. Ces avancées transforment profondément la prise en charge des pathologies lourdes comme le cancer, les maladies neurodégénératives ou les infections résistantes.
Comprendre comment ces technologies fonctionnent, quels défis elles soulèvent et quelles applications concrètes elles offrent devient essentiel pour quiconque s’intéresse à l’avenir de la santé. Cet article vous propose un tour d’horizon complet des principaux domaines où les nanotechnologies redéfinissent déjà la médecine.
Les nanoparticules au service du diagnostic précoce
La détection précoce constitue l’un des enjeux majeurs de la médecine moderne. Plus une maladie est identifiée tôt, meilleures sont les chances de la traiter efficacement. Les nanotechnologies amplifient considérablement notre capacité à repérer des signaux biologiques faibles, parfois des années avant qu’un patient ne ressente le moindre symptôme.
L’or colloïdal et les tests rapides de détection
Les nanoparticules d’or colloïdal possèdent une propriété remarquable : leur couleur change selon leur degré d’agrégation. Exploitée dans les tests à flux latéral (comme les tests de grossesse ou certains tests antigéniques), cette caractéristique permet de visualiser instantanément la présence d’une molécule cible. L’or, stable et biocompatible, offre une alternative supérieure à d’autres métaux comme l’argent ou le cuivre dans de nombreuses applications diagnostiques.
La fonctionnalisation de surface de ces nanoparticules permet de les « programmer » pour reconnaître spécifiquement un biomarqueur. Cette personnalisation transforme chaque particule en un détecteur miniature hautement sélectif, capable de signaler la présence d’une protéine pathologique, d’un fragment d’ADN viral ou d’un marqueur tumoral circulant.
Puces miniaturisées et biomarqueurs circulants
Les puces microfluidiques combinent nanotechnologies et miniaturisation pour analyser des échantillons biologiques infimes. Ces laboratoires sur puce intègrent des canaux de quelques micromètres de largeur où circulent sang, salive ou urine. Les nanoparticules fonctionnalisées y capturent les biomarqueurs circulants avec une sensibilité incomparable.
Cette approche rend possible ce qu’on appelle la biopsie liquide : plutôt que de prélever chirurgicalement un fragment de tissu suspect, une simple prise de sang suffit pour détecter l’ADN tumoral circulant, les exosomes libérés par les cellules cancéreuses ou les protéines témoins d’une inflammation chronique. Les puces à ADN et les puces à protéines exploitent l’hybridation moléculaire pour identifier simultanément des centaines de marqueurs différents.
Détecter les signaux faibles des pathologies naissantes
Les maladies chroniques et les cancers débutants émettent des signaux biologiques extrêmement ténus. Les capteurs nanotechnologiques amplifient ces signaux grâce à plusieurs stratégies :
- L’augmentation de la surface de contact entre le capteur et l’échantillon biologique
- L’utilisation de signatures moléculaires complexes plutôt qu’un biomarqueur unique, améliorant la fiabilité
- La protection des échantillons contre la dégradation pendant l’analyse
- L’optimisation de la taille des nanoparticules pour maximiser leur visibilité optique ou leur signal magnétique
Cette sensibilité accrue pose toutefois des défis techniques : éviter les faux positifs et les faux négatifs devient crucial lorsque les concentrations mesurées sont infinitésimales. La contamination croisée entre échantillons doit être rigoureusement prévenue pour garantir la fiabilité diagnostique.
L’imagerie biologique à l’échelle moléculaire
Observer ce qui se passe à l’intérieur d’une cellule vivante, suivre en temps réel la propagation d’un médicament dans l’organisme ou visualiser une tumeur de quelques millimètres : les nanotechnologies d’imagerie repoussent les limites du visible. Elles complètent les techniques classiques (IRM, scanner, échographie) en offrant une résolution moléculaire et une spécificité biologique sans précédent.
Sondes fluorescentes et quantum dots
Les quantum dots sont des nanocristaux semi-conducteurs qui émettent une lumière fluorescente intense lorsqu’ils sont excités. Contrairement aux fluorophores classiques qui blanchissent rapidement sous l’éclairage, les quantum dots maintiennent leur photostabilité pendant des heures, voire des jours. Cette propriété est fondamentale pour l’imagerie in vivo prolongée.
Leur surface peut être fonctionnalisée avec des anticorps, des peptides ou des aptamères pour cibler spécifiquement certaines cellules. Ainsi équipés, ils révèlent la distribution précise d’un récepteur membranaire, la localisation d’une protéine intracellulaire ou l’activité d’une enzyme particulière. L’imagerie en profondeur devient possible grâce à l’émission dans le proche infrarouge, une fenêtre spectrale où les tissus biologiques absorbent peu la lumière.
Deux défis persistent : gérer la toxicité cellulaire potentielle de certains quantum dots contenant des métaux lourds (cadmium), et maîtriser le phénomène de clignotement (blinking) qui interrompt momentanément leur émission lumineuse.
Imagerie multimodale et agents de contraste
L’imagerie multimodale combine plusieurs techniques d’imagerie pour obtenir à la fois des informations anatomiques et fonctionnelles. Les nanoparticules peuvent être conçues pour être visibles simultanément en IRM, en imagerie optique et en tomographie par émission de positons (PET), offrant ainsi une vision complète.
Les agents de contraste nanoparticulaires pour l’IRM présentent une relaxivité augmentée par rapport aux agents classiques. Les nanoparticules d’oxyde de fer, par exemple, modifient localement le champ magnétique et améliorent considérablement le contraste des images. Elles remplacent progressivement certains produits chimiques toxiques utilisés traditoriellement en radiologie.
L’imagerie photoacoustique illustre parfaitement l’innovation permise par les nanotechnologies : des nanoparticules absorbent la lumière laser et se dilatent thermiquement, générant des ondes ultrasonores détectables. Cette technique hybride combine la richesse du contraste optique et la profondeur de pénétration des ultrasons.
Visualisation en temps réel des processus biologiques
Suivre l’évolution d’une pathologie ou la réponse à un traitement nécessite une imagerie dynamique. Les nanosenseurs fluorescents peuvent être programmés pour réagir à leur environnement biochimique : changement de pH, présence de radicaux libres, concentration en oxygène.
Le transfert d’énergie par résonance de Förster (FRET) exploite deux fluorophores nanoparticulaires pour mesurer des distances moléculaires ou détecter des interactions protéine-protéine. L’imagerie de l’hypoxie tumorale (manque d’oxygène dans les tumeurs) guide ainsi les protocoles de radiothérapie, puisque les zones hypoxiques sont plus résistantes aux rayonnements.
La clarification optique des tissus, combinée aux nanosondes, permet désormais de rendre transparents des organes entiers pour une exploration tridimensionnelle complète, transformant notre compréhension de l’architecture tissulaire.
La vectorisation intelligente des médicaments
Délivrer un médicament précisément là où le corps en a besoin, sans affecter les tissus sains environnants, constitue l’objectif ultime de la pharmacologie moderne. Les nanotransporteurs accomplissent cette mission en encapsulant, protégeant et acheminant les principes actifs vers leur cible thérapeutique. Cette approche améliore radicalement l’indice thérapeutique des traitements lourds comme les chimiothérapies.
Nanoparticules lipidiques et protection des principes actifs
Les nanoparticules lipidiques (LNP) sont devenues célèbres grâce aux vaccins à ARN messager, mais leurs applications vont bien au-delà. Ces vésicules composées de lipides biocompatibles protègent les molécules fragiles (ARN, protéines, petits médicaments) contre la dégradation enzymatique dans le sang et l’acidité gastrique lors d’une administration orale.
Deux architectures principales dominent ce domaine :
- Liposomes : vésicules sphériques à double couche lipidique, mimant la structure des membranes cellulaires, excellentes pour encapsuler des molécules hydrophiles dans leur cœur aqueux
- Micelles polymères : assemblages de copolymères amphiphiles formant un cœur hydrophobe idéal pour solubiliser des médicaments peu solubles dans l’eau
La stabilité de ces formulations est cruciale. Il faut éviter la fuite prématurée du médicament (burst effect) avant d’atteindre la cible, tout en garantissant une libération efficace au bon endroit. La taille des particules doit être optimisée non seulement pour l’efficacité thérapeutique mais aussi pour permettre la stérilisation par filtration.
Ciblage passif et actif : atteindre la cible sans détour
Deux stratégies complémentaires guident les nanoparticules vers leur destination thérapeutique. Le ciblage passif exploite l’effet de perméabilité et rétention augmentées (effet EPR) : les vaisseaux sanguins des tumeurs, désorganisés et poreux, laissent passer les nanoparticules qui s’accumulent préférentiellement dans la masse tumorale.
Le ciblage actif va plus loin en décorant la surface des nanoparticules avec des ligands spécifiques : anticorps, peptides, sucres ou petites molécules qui reconnaissent des récepteurs surexprimés par les cellules malades. Le choix du bon ligand et l’optimisation de sa densité de surface déterminent l’efficacité du ciblage.
Des défis techniques persistent :
- Passer la barrière hémato-encéphalique pour traiter les pathologies cérébrales
- Éviter la reconnaissance par le système immunitaire (opsonisation) qui éliminerait prématurément les nanoparticules
- Contourner les mécanismes de résistance tumorale qui peuvent évoluer sous pression thérapeutique
- Séquencer précisément la libération du principe actif une fois la cible atteinte
Le ciblage magnétique constitue une alternative prometteuse : des nanoparticules magnétiques sont guidées vers l’organe malade par un champ magnétique externe appliqué depuis l’extérieur du corps. Cette approche permet même de cibler des organites intracellulaires comme les mitochondries.
Diversité des plateformes de délivrance
Au-delà des liposomes et micelles, la recherche explore une variété de nanotransporteurs aux architectures complexes. Les dendrimères sont des polymères arborescents synthétiques avec une structure parfaitement définie, offrant une capacité de chargement contrôlée et la possibilité de fonctionnaliser chaque branche.
Les nanogels combinent la flexibilité d’un hydrogel avec les avantages de la nanoéchelle : ces réseaux polymères gonflés d’eau peuvent encapsuler de grandes quantités de médicaments et les libérer en réponse à des stimuli spécifiques (pH, température, enzymes). Ils sont particulièrement adaptés aux protéines thérapeutiques qui nécessitent un environnement hydraté pour conserver leur activité.
Le choix entre vecteur organique (polymère, lipide) et inorganique (silice mésoporeuse, nanotubes de carbone, nanoparticules métalliques) dépend de nombreux critères : profil de toxicité, biodégradabilité, capacité de chargement et compatibilité avec les procédés de fabrication à échelle industrielle. Cette dernière dimension conditionne le passage du laboratoire à une production pharmaceutique réglementée.
La théranostique : combiner diagnostic et traitement
La théranostique – contraction de « thérapeutique » et « diagnostic » – représente la convergence ultime des nanotechnologies médicales. Une même nanoparticule peut simultanément révéler la localisation précise d’une tumeur et la détruire de manière ciblée. Cette approche personnalise le traitement en temps réel selon la réponse observée.
L’hyperthermie magnétique : thérapie par la chaleur
Certaines nanoparticules magnétiques, lorsqu’elles sont soumises à un champ magnétique alternatif, génèrent de la chaleur par friction interne. Ce phénomène d’hyperthermie peut élever localement la température jusqu’à 42-45°C, un seuil létal pour les cellules cancéreuses mais tolérable temporairement pour les tissus sains.
Le choix du matériau magnétique est déterminant : les nanoparticules d’oxyde de fer, biocompatibles et biodégradables, sont privilégiées face au cobalt dont la toxicité pose problème. L’optimisation de la fréquence du champ magnétique externe maximise l’échauffement tout en limitant la pénétration dans les tissus sains périphériques.
L’administration peut se faire par injection directe dans la tumeur ou par voie sanguine avec ciblage actif. La seconde approche exige une maîtrise parfaite pour prévenir l’agrégation vasculaire qui pourrait provoquer une embolie. La particule théranostique transporte également un agent de contraste IRM, permettant de suivre sa distribution et de vérifier le bon ciblage avant d’activer le traitement thermique.
Suivre et traiter : la médecine personnalisée en action
Les plateformes théranostiques intègrent typiquement trois fonctions : imagerie pour localiser la maladie, délivrance ciblée du médicament, et monitoring pour évaluer l’efficacité thérapeutique. Cette triple capacité transforme radicalement le parcours de soins.
Par exemple, une nanoparticule peut contenir simultanément un agent de contraste pour l’imagerie nucléaire (PET), un médicament anticancéreux et un fluorophore pour le suivi optique. Le clinicien visualise d’abord la biodistribution par imagerie PET, confirme l’accumulation tumorale, puis déclenche la libération du médicament par un stimulus externe (laser, ultrasons, variation de pH). Le fluorophore permet ensuite de suivre en temps réel l’effet thérapeutique.
Cette stratégie intégrée réduit les doses nécessaires, limite les effets secondaires et permet d’adapter immédiatement le protocole si la réponse est insuffisante. Elle incarne la promesse d’une médecine de précision où chaque patient reçoit le traitement optimal, ajusté en continu selon sa réponse individuelle.
Les nanotechnologies médicales ont dépassé le stade du concept pour s’imposer progressivement dans la pratique clinique. Du diagnostic ultra-précoce à la thérapie guidée par imagerie, elles offrent des outils d’une précision et d’une efficacité sans précédent. Leur développement soulève certes des questions scientifiques, réglementaires et éthiques – notamment concernant la toxicité à long terme, la biodistribution ou le coût – mais les bénéfices potentiels pour les patients justifient largement les investissements en recherche. Comprendre ces technologies, leurs principes, leurs applications et leurs limites devient indispensable pour appréhender l’évolution de la médecine et faire des choix éclairés, que l’on soit professionnel de santé, chercheur, décideur ou simplement citoyen attentif aux enjeux de santé publique.

Comment les techniques d’imagerie moléculaire permettent-elles de voir un médicament agir en temps réel ?
Visualiser l’action d’un médicament en temps réel transforme le chercheur d’un simple observateur en un véritable metteur en scène du vivant, capable de décrypter les chorégraphies moléculaires invisibles. Le choix de la technique (FRET, BRET, TEP) impose des compromis fondamentaux…
Lire la suite
Pourquoi les agents de contraste nanostructurés sont l’avenir de l’IRM sans Gadolinium ?
En tant que professionnels de santé, nous pensons souvent au remplacement du gadolinium comme un simple changement de produit. La réalité est plus profonde : les agents de contraste nanostructurés ne sont pas une simple alternative, mais une refonte complète…
Lire la suite
Comment les nanoparticules magnétiques brûlent-elles les tumeurs de l’intérieur (hyperthermie) ?
L’efficacité clinique de l’hyperthermie magnétique ne repose pas sur la simple capacité à chauffer, mais sur une maîtrise fine d’arbitrages physiques, chimiques et biologiques complexes. La sélection du champ magnétique et des particules est un compromis constant entre le pouvoir…
Lire la suite
Imagerie nanotechnologique : comment elle permet de trancher les dilemmes diagnostiques impossibles
L’imagerie nanotechnologique ne vise pas seulement à produire de plus belles images, mais à fournir l’information cruciale pour prendre la bonne décision clinique face à l’incertitude. La fusion de modalités comme l’IRM et la fluorescence permet de réduire drastiquement le…
Lire la suite
Comment la vectorisation de médicaments révolutionne-t-elle la chimiothérapie ?
L’efficacité des chimiothérapies ciblées ne dépend pas de la puissance brute du médicament, mais de l’intelligence stratégique de son système de livraison (le vecteur). La sélection d’une cible moléculaire unique à la tumeur via un diagnostic compagnon est un prérequis…
Lire la suite
Dendrimères, liposomes ou nanoparticules d’or : quel nanovecteur pour quelle thérapie ?
Le nanovecteur parfait n’existe pas ; le succès d’une thérapie ciblée réside dans le choix du bon compromis technologique. Les dendrimères offrent une charge médicamenteuse multiple et une grande stabilité, mais leur capacité d’emport reste limitée. Les liposomes, leaders du…
Lire la suite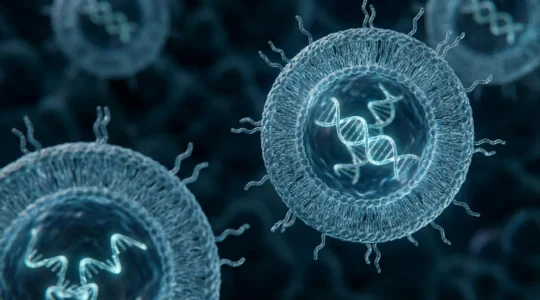
Pourquoi l’encapsulation de principes actifs est-elle la clé des vaccins à ARN messager ?
L’efficacité d’un principe actif encapsulé ne réside pas dans la robustesse de sa capsule, mais dans la conception intelligente de ses points de faiblesse contrôlés. La stabilité d’une nanoparticule lipidique (LNP) est un équilibre dynamique supramoléculaire, pas une simple enveloppe…
Lire la suite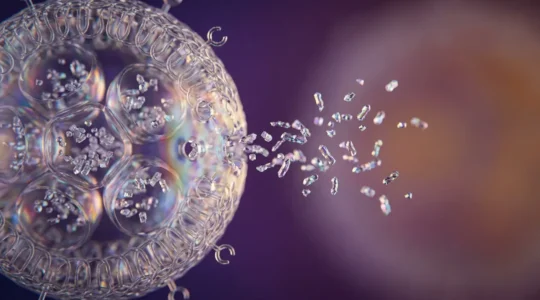
Comment la vectorisation de médicaments transforme-t-elle des poisons en remèdes ciblés ?
Le succès de la vectorisation de médicaments ne réside pas dans la conception d’une « balle magique », mais dans la maîtrise d’une chaîne de compromis pharmacocinétiques à chaque étape du parcours du nanovecteur dans l’organisme. L’efficacité ne dépend pas seulement du…
Lire la suite
Biomarqueurs nanométriques : pourquoi traquer l’infiniment petit redéfinit la médecine préventive ?
La véritable révolution des biomarqueurs nanométriques n’est pas la détection de signaux faibles, mais la maîtrise de la chaîne de valeur complexe qu’ils imposent, de la validation scientifique à la viabilité économique. La sensibilité femtomolaire des nouvelles technologies permet de…
Lire la suite
Comment les biopuces réduisent-elles le coût des analyses génétiques de 50% ?
La réduction de 50% des coûts via les biopuces ne dépend pas de la technologie seule, mais de la maîtrise rigoureuse de ses points de défaillance opérationnels. Le rendement de production des wafers et la précision des protocoles de lavage…
Lire la suite